La 26e CROI a lieu à Seattle, Etats Unis. Troisième jour de conférence. Au menu des plénières sur la pédiatrie et l’épidémiologie moléculaire, de l’hépatite C et plein de recherche fondamentale.
Deuxième plénière de mercredi : L’utilisation de l’épidémiologie moléculaire en santé publique
Certes, Antony Fauci nous a fait l’annonce du programme de mobilisation des Etats Unis pour mettre fin au sida en 10 ans. Certes, il y avait surtout dans son allocution des phrases d’encouragement à la mobilisation mais peu de description de moyens ou de méthode. Mais il nous avait bien expliqué que ce programme était la création des agences publiques de santé. Et voilà que ce mercredi matin, nous découvrons une des facettes de ce plan, celle du centre de contrôle des maladies et de la prévention, le CDC, présenté par Alexandra M. Oster.
Ce dont la chercheuse en santé publique va nous parler ce matin, ce sont des outils que le CDC a mis en place pour ciseler les interventions en prévention au mieux grâce au système de surveillance du CDC. L’épidémiologie moléculaire, puisque c’est de cela qu’il s’agit, permet de détecter où et quand une flambée épidémique se déclenche en étudiant ce que l’on nomme des grappes de transmission. Leur détection revient à déceler les failles de la prévention et permet de déclencher des interventions adaptées et ciblées. Elle utilise pour cela les tests de résistance génotypiques qui sont réalisés de manière systématique lors des diagnostics de nouvelles infections au VIH.
La transmission du VIH a lieu au sein de réseaux d’individus en relation à travers les rencontres sexuelles ou l’usage de drogue. Détecter ces réseaux lorsqu’il se produit une flambée épidémique permet d’agir pour soigner les personnes et prévenir les nouvelles infections. Un réseau est composé de personnes diagnostiquées, de personnes infectées mais non diagnostiquées, et de personnes non infectées, certaines à haut risque d’infection. Identifier un réseau permet des interventions auprès des bonnes personnes au bon moment avec les outils adaptés. L’épidémiologie traditionnelle permet de détecter la dynamique d’une épidémie et de réagir globalement sur l’ensemble des personnes concernées. Mais le VIH nous oppose d’autres défis. Le délai entre infection et diagnostic, de 3 ans en moyenne aux Etats Unis, la mobilité de la population et la concentration de l’épidémie dans certaines régions complique la donne (des paramètres en gros identiques à la France). Les analyses moléculaires qui ont été utilisées depuis longtemps dans d’autres recherches épidémiologiques de la médecine avec succès sont utilisées dans le cadre de l’infection à VIH depuis un certain temps déjà. Ce type d’analyse a été introduit à travers les tests de résistance aux antirétroviraux et font donc partie, à ce titre, des tests utilisés en routine pour tous les patients dans de nombreux pays. Si ces tests sont utiles pour le suivi individuel, ils sont aussi transmis et analysés par les agences de santé publique avec un objectif d’épidémiologie. Utilisé au départ pour la surveillance de la dissémination des résistances, elles sont d’une grande aide en ce qu’elles renseignent aussi sur la localisation géographique des contaminations. Mais ces analyses génétiques des virus peuvent aussi être mises à profit pour construire des arbres phylogénétiques. Ces analyses consistent à étudier la proximité génétique et constituent en quelque sorte un arbre généalogique dans lequel on représente la distance génétique des virus analysés. Cela permet donc de recréer les réseaux de transmission entre individus porteurs de ces souches virales autant en terme de proximité génétique (A transmet à B qui transmet à C) que de situation dans le temps (le virus de A est plus ancien que le virus de B).
Tout ce processus est le résultat de nombreuses années de recherche apportant progressivement les éléments nécessaires à la construction du dispositif tel qu’il existe aujourd’hui.
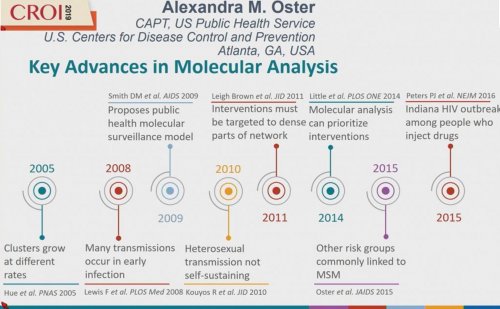
Mais parallèlement, le CDC a aussi construit son dispositif de surveillance au fil du temps selon les besoins et la disponibilité progressive des outils. Ainsi en 1997, il mettait en place le système de surveillance des résistances et la banque de données ainsi collectées. En 2013, le dispositif était complété par la création de la surveillance moléculaire étendue à l’analyse des schémas de transmissions, tout ceci permis par la mise en place de la transmission électronique des données depuis les laboratoires d’analyse. Pour autant, l’importante augmentation du volume de données fut un défi en matière de traitement pour atteindre l’objectif visé.
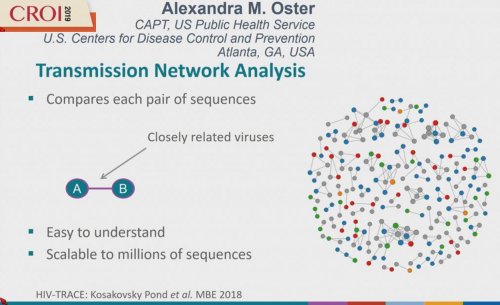
En effet, l’analyse de réseaux consiste, lorsqu’une nouvelle séquence est entrée (une nouvelle contamination) à rechercher dans la base la proximité génétique par comparaison à toutes les séquences de la base. On peut ainsi placer chaque individu au sein d’un réseau de transmission et avoir une vision d’ensemble des réseaux existants. Si ces diagrammes sont intéressants et faciles à comprendre, ils sont aussi à utiliser avec précaution car sans la compréhension scientifique de leur sens, ils peuvent être facilement mal interprétés, suggérant par exemples des données actuelles là où de grands intervalles de temps peuvent exister.
C’est l’histoire d’une flambée épidémique en Indiana en 2015 (relaté dans notre article « CROI 2016 – Boston – n°4 – Dernière journée ») qui a poussé le CDC à imaginer l’utilisation de ces données dans une approche prospective. Le premier exemple d’une telle utilisation eut lieu en Colombie Britannique (CANADA) lors de la découverte d’une série de transmission de virus résistants liés génétiquement. L’intervention mise en place auprès des personnes atteintes a permis de réduire rapidement la dissémination. C’est ainsi qu’en 2016 le CDC a mis en place une analyse systématique en routine. Compte tenu du volume de données à traiter, elle a été limitée aux nouveaux diagnostics. Les premières données ont rapidement permis d’observer que les transmissions au sein des grappes étaient largement plus importantes que l’incidence moyenne. Il a aussi été observé que l’essentiel des grappes étaient dans la population HSH. Il a été plus difficile d’identifier des grappes parmi les usagers de drogue et il est certain qu’avec les méthodes classiques en épidémiologie il aurait été impossible de détecter de rapides flambées de transmission.
Dans l’état actuel, la base de données comprend environ 40% des séquences, soit 340000 au total. Le temps de transmission de nouvelles séquences est de quelques semaines. On a identifié jusque là 145 grappes de transmission prioritaires. Les autorités sanitaires locales et au niveau des Etats ont le devoir et l’autorité pour répondre au besoin. Les outils construits permettent l’analyse quasiment en temps réel et les résultats peuvent être exploités par des personnes pas nécessairement formées techniquement. Des autorités locales ou des services de santé peuvent donc facilement construire des réponses adaptées face à l’apparition de grappes de transmission identifiées dans leur périmètre d’intervention.
Les outils d’intervention utilisés sont classiques. Ce sont les services partenaires traditionnels aussi bien que l’utilisation des réseaux sociaux qui permettent de proposer le dépistage, la PrEP, les programmes d’échange de seringue, la mise en relation avec le système de santé pour une prise en charge rapide. Et ce, de manière ciblée. La chercheuse présente quelques exemples récents de quelques interventions dans un groupe identifié de latinos HSH à San Diego / Texas, dans un groupe important de HSH en progression à Chicago / Michigan, lors d’une alerte de multiples contaminations d’usagers de drogue dans le Maryland. Mais ces expériences font aussi ressortir les questions essentielles que ce dispositif récent pose. Comment identifier les grappes de transmission qui sont importantes ? Comment adapter au mieux la réponse à l’émergence d’une grappe ? Comment mesurer l’impact des mesures entreprises ? Le CDC est engagé avec le NIH dans les recherches pour résoudre ces questions.
Le processus engagé est de transformer la détection de grappes en formation en réponses adaptées pour le plus grand bénéfice de la santé des personnes. Cependant ce système n’est pas sans risque d’effets indésirables inattendus. Le CDC entend minimiser au mieux ces effets. Les communautés sont conscientes que la technique d’épidémiologie moléculaire permet d’identifier le sens de la transmission et donc peuvent potentiellement être utilisées pour des poursuites. Les lois prévoient la condamnation de personnes qui exposent les autres ou qui ne dévoilent pas leur statut sérologique même en l’absence de transmission effective et quel que soit l’état de la charge virale. Les données de l’épidémiologie moléculaire peuvent donc potentiellement être utilisées dans ce type de poursuites judiciaires. Mais cela n’a rien à voir avec la science et ces lois ignorent les règles de la prévention. Mais pour autant la fiabilité des données n’est pas suffisante pour servir de preuve absolue de ce qui s’est passé et le système est avant tout conçu pour servir la santé publique et apporter de l’aide aux personnes qui en ont besoin. C’est pourquoi le CDC est engagé dans la protection des données des personnes et se défend de leur utilisation à d’autres fins que la santé publique. Il a mis en place ds procédures de protection des données très strictes. Les communautés sont susceptibles de se servir de telles données pour stigmatiser ou discriminer des groupes concernés par les flambées de transmission rapides. Il est clair que le CDC a pour but d’empêcher ce type d’usage. Les règles éthiques promues par l’OMS et l’ONUSIDA sont claires, la collecte de données épidémiologiques n’est justifiée que si leur usage est destiné au bénéfice de la population. C’est aussi la raison pour laquelle le CDC a engagé des représentants communautaires pour exprimer leurs besoins et définir ensemble nos buts.
En conclusion, la technique de détection de grappes de transmission et l’intervention qui en découle sont des outils pour mettre fin à l’épidémie de VIH. Les tests de résistance sont utiles à la fois pour la prise en charge des personnes et pour permettre d’arrêter les contaminations. L’analyse moléculaire pour détecter les grappes permet une identification rapide des flambées épidémiques. L’identification d’une telle grappe signale un défaut dans le service de prévention qui doit être corrigé par une intervention appropriée pour éviter de nouvelles transmissions.

Archives :
Nous vous rendons compte de nos découvertes au fil de la semaine de cette CROI 2019 à Seattle. Mais sachez que de toute manière toutes les sessions de la conférence sont revisitables sur le site internet site de la CROI en intégralité.
C’est juste en anglais et parfois ardu à suivre. Mais nous serons là pour vous proposer les clés de décodage de cette passionnante rencontre scientifique de haut niveau.
