Pistes vers la rémission :
Priorités en matière de recherches et de plaidoyer
C’est à l’occasion de cette 24ème conférence mondiale AIDS 2022 qui se tient à Montréal, CANADA que nous suivons les discussions et présentations passionnantes de ce nouveau forum « HIV Cure ». Nous savions depuis le début de la pandémie de VIH/SIDA que pour y mettre fin, la coordination et la coopération des différents acteurs de cette lutte mondiale en passant par les personnes concernées vivant avec le virus jusqu’aux scientifiques, médecins, cliniciens et décideurs est plus que vitale. Après avoir couvert le forum HIV/HBV Cure à l’IAS 2019 Mexico (voir notre article), nous confirmons que cette dynamique reste la priorité et motive les actions et projets du consortium international vers la rémission et/ou le remède contre le VIH « HIV cure » en anglais. Cette fois-ci, les orateurs ont démontré leur volonté de s’adresser, par des présentations claires et compréhensibles, aux personnes non-scientifiques. Merci.
« HIV Cure » ou la rémission virologique c’est quoi au juste ?
Cette nouvelle édition réunit non seulement les experts scientifiques mais aussi les représentants des communautés impactées par le Virus de l’Immunodéficience Humaine responsable du Syndrome d’Immunodéficience Acquise (VIH/SIDA). Les organisateurs innovent par une approche interactive avec le public présent. La question posée est la suivante : qu’entendez-vous par « HIV cure » ? Est-ce le fait d’avoir une charge virale sanguine très basse sous le seuil de détection des tests virologiques (ou charge virale dite indétectable) ? Ou est-ce le fait de ne plus avoir besoin de prendre de traitements antirétroviraux bien que je vive avec le VIH ? Ou alors « HIV Cure » signifie-t-elle l’éradication complète du virus de mon organisme ? L’objectif affiché ici est de faire évoluer ou non la compréhension du public et surtout d’informer, d’éduquer pour qu’ensuite les acteurs communautaires soient en mesure de transmettre et de partager les messages une fois le forum terminé.
Malgré le succès des antirétroviraux (ARV) pour les personnes vivant avec le VIH, (PVVIH), un traitement à vie est nécessaire. La recherche galénique progresse au point de proposer des formes d’ARV injectables à longue durée d’action. Mais il n’y a toujours pas de remède alternatif actuellement permettant de vivre sans ARV. Cela est dû à la biologie du VIH qui se présente sous deux formes : une forme réplicative et une forme latente, cachée au sein de cellules infectées dites « réservoirs ». En effet, le VIH peut s’intégrer dans le génome de l’hôte et persister pendant toute la durée de vie de la cellule infectée. Dans le pire des cas ces cellules se mettent à proliférer et amplifier ainsi la taille du réservoir viral. Ces cellules réservoirs de manière latente ne sont pas reconnues comme étrangères car elles sont en grande partie silencieuses sur le plan de la transcription virale. Dans ces cellules réservoirs le VIH latent est capable de se répliquer dès l’activation de la cellule, entraînant alors la résurgence de l’infection et la détectabilité de la charge virale sanguine une fois la prise d’ARV arrêtée (Ref Nature). C’est parce que nous ne savons pas comment faire pour éliminer le réservoir de VIH latent qu’il est encore aujourd’hui quasi impossible de guérir de l’infection par le VIH. Tout au mieux peut-on espérer de se rapprocher de la rémission : vivre avec très peu de réservoir viral sans avoir à prendre d’ARV et sans prendre de risque d’exposer nos partenaires au virus. Avec une combinaison d’activateurs immunitaires, d’anticorps neutralisants et de vaccins thérapeutiques, certains modèles de primates non humains (ex, les macaques asiatiques), infectés par le SIV (forme simienne du VIH) ont été guéris, ce qui donne de l’optimisme pour ces approches actuellement évaluées dans des essais cliniques sur l’homme. L’utilisation in vivo d’outils d’édition ou de modification de gènes pour cibler le virus, renforcer l’immunité ou protéger les cellules contre l’infection est également prometteuse pour les futures stratégies de guérison du VIH. Lors de ce forum « HIV Cure », sont discutés les progrès liés menant à la rémission, voire à la guérison après l’éradication complète de tout réservoir de cellules infectées par le VIH pour quatre PVVIH officiellement. La communauté scientifique et médicale est consciente … ou pas, des lacunes restantes en matière de connaissances et se réunit lors de ce forum avec les acteurs communautaires afin d’identifier les domaines de recherche et de plaidoyer prioritaires pour les cinq prochaines années. L’inclusion de tous les profils de PVVIH (femmes cis, personnes transgenres et enfants) est absolument requise dans les études en vie réelle et lors des essais cliniques.
Nous souhaitons par cet article vous transmettre les points essentiels de cette journée pour que vous puissiez vous aussi lectrices et lecteurs de reactup.fr en ligne, vous approprier l’information pour votre propre « empowerment ».
Enjeux et priorités en matière de recherches
Le Pr Sharon Lewin, qui deviendra la nouvelle présidente de l’IAS (International AIDS Society), à l’issue de la conférence AIDS 2022, débute cette journée par une présentation ayant justement pour but de combler les lacunes en matière de connaissances et d’informations. Le Pr Lewin rappelle les enjeux de ce forum à l’audience constituée des représentants de communautés touchées par le VIH et la communauté scientifique et cliniciens impliquées dans la recherche de mécanismes menant à « HIV Cure » (Figure 1).

Figure 1. Liste des enjeux et priorités en matière de recherche et de plaidoyer définie par la commuté scientifique.
Avant de poursuivre, voici un rappel du vocabulaire admis par l’ensemble des acteurs engagés dans cette initiative « HIV Cure ». Ces termes utilisés sont cruciaux pour les chercheurs, les cliniciens et les PVVIH afin de se comprendre mutuellement:
Un remède contre le VIH comprend à la fois la rémission et l’éradication. Le terme rémission est définit comme un contrôle durable du virus en l’absence de toute prise d’ARV en cours. L’éradication est l’élimination complète du virus intact et capable de se répliquer concourant au rebond de la charge virale sanguine qui redevient détectable par les tests virologiques utilisés en laboratoire.
Le terme « réservoir du VIH » dans le contexte de l’éradication ou de la rémission, représente l’ensemble de toutes les cellules infectées par le VIH capable de se répliquer à la fois dans le sang et dans différents sites anatomiques chez les personnes sous ARV. En d’autres termes, le réservoir représente toutes les sources potentielles de rebond viral dans le cadre d’une interruption d’ARV. Bien que la source du rebond du virus ne soit pas encore entièrement comprise, il est désormais admis maintenant que le virus peut persister sous plusieurs formes, dans plusieurs cellules et dans plusieurs sites, le système nerveux central restant peu étudié pour des raisons compréhensibles (Figure 2).
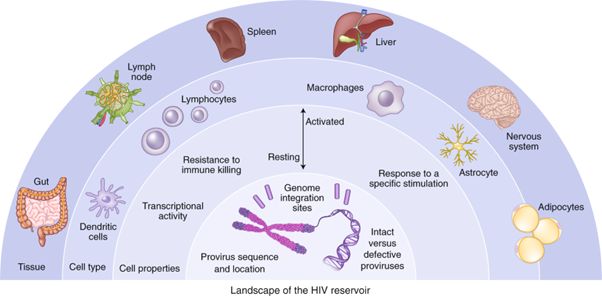
Figure 2. Le réservoir du VIH. Il peut être défini, notamment : (1) par les emplacements anatomiques et micro anatomiques, (2) par le type de cellule (par exemple, cellule cible T CD4+ ou macrophage CD4+), (3) par le profil fonctionnel de la cellule (activée ou au repos), (4) par le pool de provirus (virus intégré) avec un profil fonctionnel particulier (par exemple, résistant à des molécules antivirales produites par l’organisme tel que l’interféron-alpha) ou (5) par un événement déclencheur (par exemple, réponse à la stimulation avec un antigène c’est-à-dire un petit fragment de protéine virale particulier), et (6) par le site d’intégration dans le génome cellulaire, caractéristiques du virus responsable du rebond de la charge virale. Source : Steven G. Deeks et collaborateurs, Nature Medicine, Décembre 2021, pages 2085-2098. Image présentée tout au long de cette journée.
Les priorités de la recherche
Comme expliqué dans notre dernier article sur le forum HIV/HBV Cure à la conférence IAS2019 à México, l’un des objectifs des chercheurs est de poursuivre l’identification de marqueurs cellulaires permettant de mieux identifier, quantifier et localiser les cellules infectées par du VIH intégré et latent. Un marqueur signifie ici l’expression d’une molécule spécifiquement par la cellule infectée correspondant aux critères d’une cellule dite réservoir. L’ADN (génome viral intégré dans le génome cellulaire après l’étape de rétrotranscription de l’ARN viral après infection de la cellule) du VIH peut être détecté dans les lymphocytes T CD4+ du sang et des tissus lymphoïdes chez presque toutes les PVVIH sous ARV. Ces génomes viraux sont pour beaucoup défectueux. Seule une petite proportion (moins de 5%) semble être intacte et potentiellement compétente pour la réplication et la multiplication du VIH. Mais le réservoir viral va au-delà des lymphocytes T CD4+ circulants dans le sang, il comprend également les cellules localisées dans les tissus profonds difficilement accessible pour la recherche scientifique et/ou clinique. In vitro, dans un tube à essai de laboratoire, le VIH s’intègre préférentiellement dans les parties des chromosomes dont la structure est dite transcriptionnellement active permettant à toute la machinerie du noyau de la cellule d’accéder au génome intégré du VIH. Ce dernier profite ainsi d’un environnement favorable à sa propre réplication et multiplication. Cependant, chez les PVVIH sous ARV, de nombreux provirus (définis comme des virus intégrés dans le génome de l’hôte), y compris des virus intacts, ont été identifiés dans des régions génomiques « silencieuses » des chromosomes. Ces « déserts génétiques » où la structure du chromosome est ultra dense et non accessible à la machinerie cellulaire, limite ou empêche la réactivation ou le réveil des provirus VIH intégré sous forme latente. Et ceci rend extrêmement complexe toute éradication complète du VIH et donc des réservoirs viraux à l’heure actuelle. L’identification de marqueurs cellulaires facilitant spécifiquement le ciblage du réservoir viral ouvrirait la voie à de nouvelles pistes de recherches pour réduire la taille du réservoir viral et d’atteindre la rémission.
D’autres études évaluant les stratégies dites « poke and clear », « block and lock » ou « reduce and control » sont aussi en cours.
Brièvement, le « poke and clear » (anciennement « shock and kill ») implique l’utilisation de médicaments permettant l’inversion de la phase de latence virale et donc de réveiller le virus « endormi » dans les cellules infectées. Une deuxième étape faciliterait la destruction des cellules infectées après les avoir activées. En effet, le VIH a besoin de l’activation cellulaire pour se multiplier et permettre ainsi la reconnaissance de la cellule infectée par le système immunitaire. Le « block and lock » est une stratégie inverse. Comme nous l’explique Melanie Ott dans sa présentation, cette approche chercherait à endormir complètement le VIH intégré dans le noyau de la cellule infectée et de faire en sorte qu’il ne puisse se réveiller quel que soit l’état d’activation de la cellule. En d’autres termes cette piste de recherche induirait une super latence virale. Enfin le « reduce and control » aurait pour objectif de réduire la taille du réservoir viral afin de permettre au système immunitaire de prendre le contrôle sans avoir recours aux ARV.
Dans le cas du « reduce and control », les scientifiques développent actuellement 3 méthodes prometteuses. Les bnAbs, (broadly neutralizing Antibodies ou anticorps largement neutralisants), les thérapies cellulaires et de génie génétique sont les agents moléculaires et techniques retenues.
Les bnAbs sont des anticorps que produit le système immunitaire et qui vont reconnaitre un petit fragment du VIH et neutraliser le virus en l’empêchant d’infecter de nouvelles cellules. Des bnAbs ont été identifiés chez des PVVIH présentant des réponses immunitaires efficaces. Il est possible en laboratoire de les synthétiser et de les modifier pour les rendre plus robustes dans leur action antivirale et à plus longue durée d’action (plus de temps pour perdre 50% de la totalité des bnAbs). Différents bnAbs sont actuellement testés en combinaison dans des projets de recherche clinique dans le cadre d’interruption de prise d’ARV programmée. In vitro dans des tubes à essai en laboratoire leur efficacité n’est plus à démontrer mais il faut maintenant prouver que cette approche fonctionnerait en vie réelle après injections chez des PVVIH.
En ce qui concerne les thérapies cellulaires et de génie génétique, plusieurs approches novatrices sont basées sur la modification du génome de manière ex vivo ou in vivo. Par ex vivo nous entendons les techniques où les cellules d’intérêt du patient sont prélevées, modifiées en laboratoire puis réintroduites. Par in vivo, des nanomolécules sont injectées puis vont cibler les gènes à modifier dans les cellules cibles. Dans le cadre de l’approche in vivo, des chercheurs tentent d’utiliser la technologie CRISPR/Cas9 dite des ciseaux moléculaires pour couper le gène codant l’expression du corécepteur CCR5 nécessaire à l’entrée du VIH dans la cellule TCD4+. Grâce à cette technologie, le CCR5 synthétisé serait tronqué d’une partie de sa structure devenant alors inutilisable par le VIH. Ceci préviendrait toute nouvelle infection et donc contribuerait à réduire la taille du réservoir viral. D’autres technologies sont actuellement mises au point dans l’optique de modifier le génome. Il s’agit non plus d’utiliser CRISPR/cas9 mais d’autres enzymes telles que les nucléases à doigt de Zinc et les nucléases effectrices de type activateur de la transcription. Pour des raisons que vous comprendrez nous n’irons pas plus loin dans les détails. Enfin en ce qui concerne la technologie des lymphocytes T porteurs de récepteurs antigéniques chimériques (CARTcells) nous vous renvoyons à l’article Forum HIV HBV Cure IAS2019. Dans ce cadre, les lymphocytes T CD8+ (lymphocytes tueurs) du patient sont prélevés puis modifier en laboratoire afin de leur faire exprimer un récepteur chimérique pouvant reconnaitre plus efficacement les cellules infectées par le VIH. Une fois chimérisés les lymphocytes T CD8+ sont réinjectés aux patients. Les études chez les PVVIH sont rares et aucune étude n’a pu encore prouver en vie réelle leur efficacité pour atteindre la rémission voire l’éradication complète du réservoir viral. Le principal obstacle à la recherche est la localisation des cellules constituant le réservoir viral. Il ne suffit donc pas d’injecter des super lymphocytes T CD8+ tueurs mais encore faut-il qu’ils aillent au bon endroit dans l’organisme sans déclencher des effets collatéraux au risque d’induire des effets indésirables pouvant nuire à la qualité de vie des PVVIH.
Les 4 cas de guérison avérée
A ce jour, seulement 4 personnes adultes sont officiellement « guéries ou ayant atteint le stade de rémission » de l’infection par le VIH comme nous le rappelle dans leurs présentations les Dr Kumitaa Theva Das et le Pr Deborah Persaud (Figure 3). Cette dernière dirige l’équipe de recherche américaine à New-York qui a pu guérir pour la première fois, une femme vivant avec le VIH. S’appuyant sur les succès passés, ainsi que sur les échecs, dans le domaine de la recherche sur « HIV Cure », ces scientifiques ont utilisé une méthode de greffe de cellules souches (möelle osseuse et de sang de cordon ombilical). Cette patiente, ex PVVIH, a ainsi rejoins les trois hommes que les scientifiques ont guéris, ou très probablement en rémission, du VIH.

Figure 3. Liste des personnes et groupe de PVVIH ayant atteint le stade de rémission/guérison ou décrites comme super élites contrôleurs, élites contrôleurs et contrôleurs après arrêt de traitements ARV (Cohorte française Visconti)
Dans les 3 premier cas de ce qui a finalement été considéré comme une guérison réussie du VIH, les cliniciens investigateurs avaient traité leurs patients dans le cadre d’une prise en charge pour une leucémie myéloïde aiguë (LAM en anglais). Ils avaient reçu une greffe de cellules souches (möelle osseuse) d’un donneur qui avait une anomalie génétique rare (délétion delta 32 du corécepteur CCR5) qui accorde aux cellules immunitaires d’être naturellement résistant à l’infection par le VIH. La stratégie dans le cas de Timothy Brown, (décédé en 2020 de complications dues à la LAM) qui a été rendue publique pour la première fois en 2008, a depuis été reproduite avec succès chez deux autres personnes (patients de Londres et de Dusselforf). Mais il a également échoué pour d’autres patients et il est bien dommage de ne pas savoir pourquoi la technique a ainsi échoué.
Ce processus thérapeutique vise à remplacer le système immunitaire d’un individu par celui d’une autre personne, en traitant son cancer tout en éradiquant le réservoir de VIH. Premièrement, les médecins doivent détruire le système immunitaire d’origine par chimiothérapie (parfois par irradiation). L’objectif ici recherché est que la chimiothréapie détruise également autant de cellules immunitaires que possible qui hébergent le VIH latent malgré la prise d’ARV. Ensuite, à condition que les cellules souches résistantes au VIH (CCR5 delta 32) transplantées se greffent correctement, les nouvelles particules virales qui pourraient émerger de toutes les cellules infectées restantes du patient receveur seront incapables d’infecter les cellules du système immunitaires du donneur qui se sont greffées et amplifiées chez les patients receveurs. Il semblerait que le point commun aux 4 patients ainsi guéris ait été le déclenchement d’un phénomène dangereux pour les patients receveurs : le rejet des cellules du donneur par les cellules greffées (GVH « graft versus host disease ou maladie du greffon). En d’autres termes les cellules greffées sont activées car elles reconnaissent les cellules du patient receveur comme étrangères et se mettent donc en ordre de marche pour les détruire. Cette maladie du greffon peut être fatale pour le patient receveur qui doit être traité avec des immunosuppresseurs pour limiter ce phénomène de rejet. Paradoxalement c’est peut-être là que réside le mécanisme de guérison du VIH. Les cellules greffées ainsi activées se mettraient à éradiquer les quelques cellules infectées par le VIH résiduelles chez le patient receveur. C’est pour cette raison et les risques encourus que le Pr Deborah insiste qu’il serait contraire à l’éthique, de tenter de guérir du VIH par une greffe de cellules souches – une procédure toxique, parfois fatale – chez une personne qui n’a pas un cancer potentiellement mortel.
Les super élites et les élites contrôleurs du VIH
Le Dr Gabriela Turk et le Pr Javier Martinez-Picado nous présentent également l’état des connaissances chez les patients dits super elite et elite controleurs du VIH.
Dans le premier cas il s’agit de deux femmes (Patiente de San Francisco et Patiente Esperanza) dont le propre système immunitaire a de manière tout à fait extraordinaire, vaincu l’infection par le VIH. Chez ces deux patientes l’infection par le VIH a pu être diagnostiquée mais elles présentaient une séroconversion incomplète (western blot faible ou incomplet) en primo-infection (phase aiguë de l’infection), le maintien d’un niveau élevé de T CD4+ et de faibles fréquences de lymphocytes T CD8+ spécifiques du VIH, ceci en l’absence de toute prise d’ARV. Après plus de 10 années de suivi sans ARV, ces personnes semblent contrôler de manière extrême l’infection par le VIH. A ce jour il n’a pas été possible de détecter la moindre particule virale de VIH infectieuse capable de se multiplier lors des tests in vitro en laboratoire.
Dans le deuxième cas, les patients présentent une séroconversion complète, un réservoir viral bas et des charges virales sanguines très faibles voire indétectables. Contrairement aux deux premières patientes citées, il est facile de détecter des particules virales de VIH infectieuses chez les élites contrôleurs. La variabilité génétique des virus isolés est faible témoignant d’une réplication virale très résiduelle associée à une faible quantité de réservoir viral. Les patients élites contrôleurs sont un groupe hétérogène et pour l’instant aucun mécanisme précis n’a pu être identifié pour expliquer leur statut commun. L’explication est très probablement multi-factorielle. Toutefois il semblerait que l’immunité innée impliquant les cellules dites « Natural Killer NK » soit forte ainsi que des lymphocytes T CD8+ spécifiques du VIH efficaces, en réponse à l’infection.Le Pr Javier Martinez-Picado poursuit en nous indiquant que les virus isolés chez les élites contôleurs présentent une protéine enveloppe avec une plus faible capacité fonctionnelle à fusionner avec la membrane de la cellule ciblée par le VIH. Il poursuit par des resultats montrant que les anticorps isolés chez ces individus sont deux fois plus réactifs que ceux retrouvés chez les patients ayant reçus une transplantation de cellules CCR5 delta 32. Ceci s’explique par la présence d’antigènes viraux résiduels chez les élites contrôleurs contrairement aux patients ayant atteint le stade de rémission/guérison hautement probable. Mais les résultats les plus surprenant sont ceux décrivant la taille du réservoir viral entre les patientes super élites contrôleurs, les élites contrôleurs en comparaison avec les PVVIH sous ARV. La taille du réservoir viral mesuré ici par la quantité de provirus intégré (nombre de copies d’ADN du VIH par million de cellules sanguines circulantes) est 100 fois plus faible chez les super élites contôleurs en comparaison de la taille du réservoir chez les patients élites contôleurs. Les PVVIH sous ARV ont une taille de réservoir 10 fois plus élevée que celle observée chez les élites contrôleurs (Figure 4).

Figure 4. Présentation du Pr Javier Martinez-Picado questionnant le rôle du site d’intégration du génome du VIH dans le noyau et l’association possible avec la taille du réservoir viral chez les super élites contrôleurs, les élites contrôleurs en comparaison aux PVVIH sous traitements ARV.
Des études supplémentaires sont plus que nécessaires afin d’identifier les sites d’intégration et les mécanismes moléculaires associés à cette intégration spécifique associée à une faible taille du réservoir viral chez les super élites et les élites contrôleurs. En guise de conclusion le Pr Javier Martinez-picado pose la question suivante : est-il possible d’induire un contrôle permanent (durable) de la latence afin de prévenir toute progression vers le SIDA ?
N’oublions pas que toute avancée en matière de recherche doit aussi profiter au plus grand nombre. Jusqu’à présent nous avons abordé la population adulte plutôt masculine car les femmes et les enfants sont largement sous-représentés dans les études, même si des progrès à force de marteler lors des conférences l’absolue nécessité d’obtenir des résultats également au sein de ces populations clefs qui portent aussi un lourd fardeau.
Contrôle de la charge virale chez les enfants et les femmes.
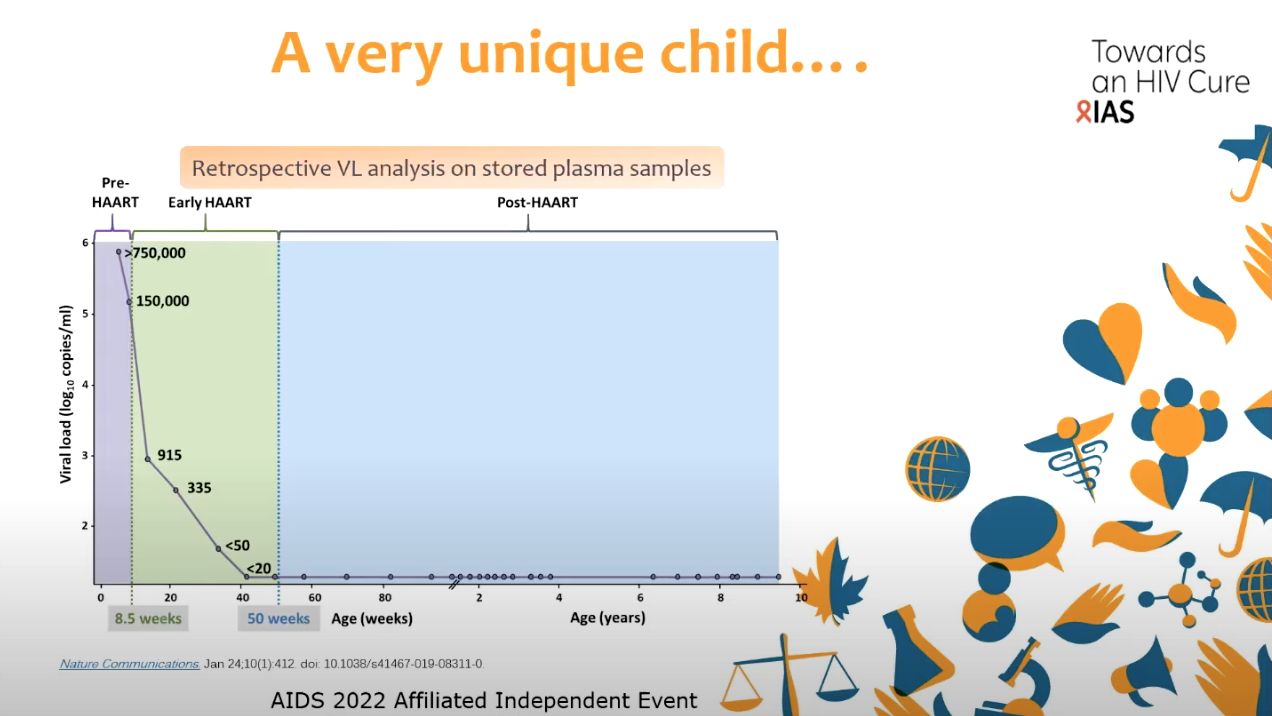
Figure 5. Évolution de la charge virale sanguine en fonction du temps après diagnostic de l’infection par le VIH, de l’enfant sud-africain ayant atteint le stade de rémission/guérison fortement probable.
Le Pr Maria Paximadis nous présentes des données récentes au sujet d’un enfant sud-africain ayant atteint le stade de rémission ou de guérison probable (Figure 5). L’enfant de neuf an infecté par le VIH à la naissance a passé la majeure partie de sa vie sans avoir besoin de traitement. L’enfant s’est retrouvé infecté par transmission de sa mère au moment de la naissance en 2007. Il avait des niveaux très élevés de VIH dans le sang (plus 6 Log 10 copies/ml de sang). Il a reçu des ARV peu après sa naissance environ à 9 semaines post-diagnostic puis après interruption du traitement à la 50ème semaine, la prise d’ARV a été interrompue. Depuis et après huit ans d’interruption de traitement cet enfant ne présente aucun symptôme ni signes de virus détectable et infectieux.
Comprendre comment l’enfant est protégé pourrait conduire à de nouveaux médicaments ou à une stratégie pour atteindre le stade de la rémission/guérison chez tous les enfants.
La thérapie antirétrovirale précoce n’était pas une pratique courante à l’époque, mais était administrée à l’enfant à partir de neuf semaines dans le cadre d’un essai clinique.
Les niveaux de virus sont devenus indétectables, le traitement a été arrêté après 40 semaines et contrairement à tous les autres participants à l’étude, le virus n’est pas revenu.
Une thérapie précoce qui attaque le virus avant qu’il ait une chance de s’établir complètement a été impliquée dans des cas de « guérison » d’enfants à deux reprises auparavant. Pour rappel, le « Mississippi Baby » a été mis sous traitement dans les 30 heures suivant sa naissance et est resté 27 mois sans traitement avant que la charge virale sanguine ne soit à nouveau détectable. Il y a eu aussi un cas en France avec une jeune patiente qui a maintenant passé plus de 12 ans sans ARV.
La recherche pédiatrique dans le cadre de l’effort pour trouver un remède conduisant à la rémission/guérison s’active. Le Pr Déborah Persaud qui a aussi contribué à ce que la patiente de New-York soit en rémission, nous présente une étude clinique en cours « IMPACT P1115 » dont l’objectif est de traiter immédiatement des nouveaux nés diagnostiqués VIH+ à leur naissance ou diagnostiqués in utero (Figure 6).

Figure 6. Présentation du rationnel de l’étude IMPACT P1115
Ces enfants sont actuellement suivis en Afrique, en Asie et en Amérique Nord/Sud. Des premiers résultats prometteurs nous sont présentés mais nous ne les détaillerons pas car ils ont été obtenus sur très peu d’enfants. Les analyses ne font que commencer et nous ne voulons pas susciter de faux espoirs à ce stade (Figure 7). Le Pr Persaud présente également brièvement une autre étude en cours qui cette fois-ci cherche à évaluer l’injection de bnAbs (les fameux anticorps neutralisants) chez 25 enfants VIH+ au Botswana (étude TALEO). Parmi les 25 enfants participant à l’étude, 44% maintienent une charge virale sanguine indétectable durant les 24 semaines de traitement par bnAbs comme traitement alternatif aux ARV. 56% des enfants n’ont pu bénéficier des bnAbs car ils n’avaient pas staibiliser leur charge virale sanguine durant les 24 semaines de traitement sous ARV avant l’interruption programmée afin de recevoir les injections de bnAbs. La recherche poursuit son cours et nous espérons avoir plus d’informations lors des prochaines conférences internationales.
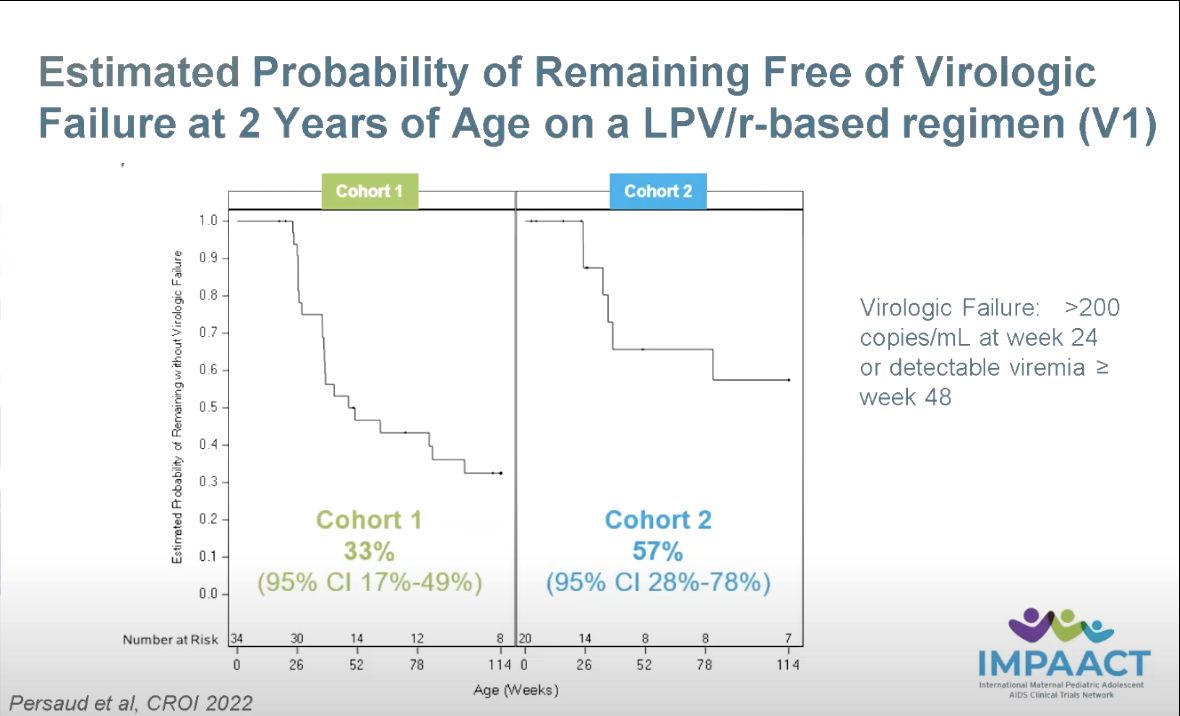
Figure7. Données préliminaires de l’étude IMPACT 1115 et probabilité estimée pour les enfants diagnostiqués VIH+ traités dès leur naissance par les ARV (Cohorte 1) ou durant la période in utero (Cohorte 2) de pouvoir contrôler leur charge virale sanguine après initiation des ARV. Plus le traitement est initié précocement (in utero versus post partum) moins le risque est élevé de sélectionner des souches de VIH résistantes aux ARV.
Enfin, le Dr Jessica Prodger discute des considérations et arguments à prendre en compte lorsqu’il s’agit d’inclure des femmes cis-genres dans les études « HIV Cure ». Tout d’abord les femmes cis-genre présentes des taux de TCD4+ et de ratio TCD4/TCD8 dans les sangs plus élevés que les hommes cis-genres. Toutefois les charges virales sanguines semblent être plus faibles que chez les hommes cis en phase précoce de l’infection par le VIH. Or les femmes progressent plus vite vers le sida, du moins elles perdent plus rapidement leur TCD4+ sanguins à charge virale sanguine identique par rapport aux hommes cis-genres. Ces disparités observées en phase précoce de l’infection seraient dues aux concentrations plus élevées d’interféron de type I (cytokine anti-virale produite après toute infection virale) par rapport à ceux quantifiés chez les hommes cis-genres. Il a été proposé que la réponse IFN-I inappropriée durant l’infection par le VIH contribuerait à une perte plus rapide des T CD4+. Des données obtenues dans les modèles de primates non humains avaient déjà montré que les singes africains naturellement infectés par leur SIV ne progressant pas vers le SIDA ont une réponse IFN-I très rapide et transitoire en comparaison aux macaques asiatiques progressant systématiquement vers la maladie et chez qui la réponse IFN-I est beaucoup plus forte et semble s’éterniser. De plus le Dr Prodger rappelle que les cycles hormonaux influent potentiellement sur l’infection par le VIH. Les œstrogènes par exemple interfèrent dans des tests in vitro en laboratoire avec les agents de réversion de la latence qui sont utilisés dans le cadre de stratégie « poke and clear » décrite plus haut dans cet article. Elle nous rappelle aussi que beaucoup de gènes codant pour des protéines impliquées dans la réponse IFN-I sont situés sur le chromosome X. Par conséquent le fait d’avoir deux XX pourrait potentiellement remettre en question des mécanismes intrinsèques menant à la rémission/guérison qui seraient identifiés chez les hommes cis-genres. Par conséquent le Dr Jessica Prodger conclue sur l’importance de lancer plus d’études spécifiques dédiées aux femmes cis-genres afin de prendre en compte leur biologie et leur propre métabolisme.
Plaidoyer pour plus d’inclusivité, d’éthique, de transparence et d’engagement communautaire
Le Pr Simon Collins (comme beaucoup d’autres speakers intervenant lors de cette journée riche en messages envers les communautés impactées par le VIH/SIDA), nous rappelle l’urgence à constamment cibler les études menées dans le cadre de cet effort international pour identifier des stratégies « HIV Cure » afin qu’elles soient le plus proche possible des besoins exprimés par les populations clefs.
La recherche visant à guérir du VIH mêle des aspects sociaux, comportementaux et éthiques critiques qui doivent être intégrés à l’agenda scientifique. Cette recherche se déroule dans des contextes sociaux et des communautés particuliers qui façonnent sa licéité et sa pertinence. En conséquence, les communautés affectées doivent être impliquées de manière significative tout au long du processus de recherche ; les facteurs sociaux et comportementaux doivent être interrogés et pris en compte car ils affectent la faisabilité de la recherche, le soutien communautaire à la recherche et le bien-être des participants et des autres parties prenantes. La recherche doit également aborder les nombreuses questions éthiques associées au développement d’une thérapie, d’autant plus que des options thérapeutiques viables sont déjà disponibles. Un financement suffisant pour la recherche sur les aspects sociaux, comportementaux et éthiques d’un traitement et pour la participation communautaire est donc essentiel.
L’engagement communautaire dans la recherche « HIV Cure » est encore sous-optimal dans de nombreux contextes, étant principalement limité à des conseils consultatifs généralement composés de personnes ayant des connaissances scientifiques. La capacité de discuter de la recherche sur la guérison du VIH et d’évaluer ses implications potentielles pour les communautés locales et mondiales doit être renforcée au sein de divers groupes communautaires. Les communautés devraient être responsabilisées et soutenues par l’éducation et l’engagement à tous les niveaux du processus de recherche pour aider à façonner le programme de recherche sur la guérison du VIH et permettre aux participants potentiels à l’étude d’avoir une voix dans la conception des essais152.
L’attention doit se concentrer sur une large représentation (par exemple, l’âge, la race et l’origine ethnique, le sexe et la sexualité, l’emplacement géographique, les comportements à risque) dans la recherche. La diversité dans la participation est essentielle lors du développement d’interventions visant l’élimination complète du VIH ou un contrôle durable sans ARV. Cela nécessite des recherches visant à comprendre les raisons de la sous-représentation de certains groupes de personnes dans la recherche sur « HIV Cure ». Par exemple, les femmes cisgenres et transgenres, ainsi que les personnes de certaines origines raciales et ethniques, sont moins susceptibles de participer à des essais cliniques dans le cadre « HIV Cure ». Cela met en évidence la nécessité d’une recherche plus nuancée et théoriquement engagée pour comprendre comment le sexe, la race et d’autres caractéristiques façonnent l’engagement dans la recherche sur la guérison/rémission. Dans le même temps, les considérations juridiques et sociales propres à chaque contexte doivent être identifiées et traitées. Par exemple, les lois locales, la stigmatisation et l’accès aux soins de santé affectent la recherche impliquant l’interruption des ARV.
Il est également nécessaire de mieux définir les considérations éthiques impliquées dans la sélection des populations d’intérêt dans lesquelles des stratégies de guérison prometteuses seront testées. Par exemple, la priorité doit-elle être donnée au test de nouvelles interventions chez les personnes qui ont commencé un traitement pendant une infection aiguë plutôt que chez celles qui ont commencé un traitement pendant une infection chronique ? Quels sont les meilleurs moyens d’identifier et de gérer les considérations éthiques dans la recherche pédiatrique sur la guérison du VIH ? De plus, quelles mesures devraient être prises pour s’assurer que le recrutement n’est pas biaisé en faveur des personnes vivant avec le VIH dans les milieux à ressources limitées ? En outre, les questions éthiques d’équité et de justice liées à la distribution d’interventions curatives sûres et efficaces doivent tenir compte de l’acceptabilité, de l’évolutivité et de la rentabilité. La pandémie de COVID-19 a soulevé des considérations uniques pour les participants à la recherche, le personnel et les communautés. Compte tenu de l’évolution rapide de la nature de la pandémie et de la disponibilité des vaccins COVID-19 et d’autres traitements, il est nécessaire de réviser et d’évaluer en permanence la sécurité et la faisabilité des efforts de recherche pour atteindre enfin la rémission/guérison chez toutes le PVVIH
Au cours de la phase de conception de l’étude, un engagement précoce est nécessaire dans les communautés où la recherche est envisagée afin de déterminer la nature et l’acceptabilité des risques liés à la recherche. De même, les perceptions des parties prenantes doivent être obtenues pour guider le développement de profils de produits cibles (les caractéristiques minimales et optimales d’une nouvelle intervention thérapeutique). Dans les études cliniques particulièrement complexes, la recherche formative devrait être utilisée pour aider à développer un processus de consentement solide et éclairé (reference Nature et présentations de tous les speakers intervenus lors de cette journée).
Conclusion
Malheureusement nous ne pouvons tout résumer ici dans cet article mais nous espérons que vous pourrez de nouveau construire votre propre avis éclairé et que vous serez convaincus de l’effort international lancé dès 2016 pour mobiliser la communauté scientifique et les décideurs ainsi que les communautés touchées par le VIH/SIDA vers l’identification de stratégies thérapeutiques visant le stade de la rémission/guérison. Au cours des prochaines conférences abordant la thématique « HIV Cure », nous nous attendons à une meilleure compréhension des réservoirs du VIH, à un nombre croissant d’essais cliniques et, espérons-le, à des rapports sur des personnes ayant obtenu une rémission à long terme avec des stratégies moins intensives et plus largement applicables que celles que nous vous avons décrites dans cet article. N’oublions pas que les coûts de telles stratégies ne permettent pas à l’heure actuelle d’en faire profiter le plus grand nombre losrque les PVVIH répondent aux critères d’inclusion.
Sur la base de la compréhension actuelle et des leçons tirées des études en cours, il est probable que des combinaisons multiples de stratégies déjà décrites puissent à moyen terme être mises en œuvre. Il est urgent que les fonds dédiés à « HIV Cure » puissent également servir à construire les infrastructures nécessaires à l’implémentation de ces stratégies prometteuses dans les pays à faibles revenus.
Enfin, des communications ouvertes et responsables sur les essais et considérant sérieusement les attentes réalistes et leurs problématiques de vie réelle des populations clefs doivent être maintenues. Nous saluons les efforts de présentation lors de cette journée. La qualité des échanges entre tous les acteurs présents le prouve. Tous les acteurs impliqués doivent se comprendre afin que le rêve d’une éradication du VIH puisse enfin devenir pour tous et toutes une réalité.
Retrouvez les autres articles de la AIDS 2022 :
- AIDS 2022 Forum HIV cure
- AIDS 2022 à Montréal, vue d’ensemble
- AIDS 2022, morceaux choisis
Retour à la page de tête :
Source
Deeks SG, Nature Medicine volume 27, pages 2085–2098 (2021)
