Il y a pléthore de thèmes de sujets et de sessions dans cette IAS 2023. Voici une sélection de certaines choses ont retenu notre attention. Il sera question du coût du contrôle de l’épidémie, à mettre en regard de la difficulté de l’implémentation. En actualité, nous avons retenu cette présentation sur un nouveau patient guéri, semble-t-il ainsi que le dernier résultat d’avancement d’un nouveau traitement, l’Islatravir. Enfin, dans le chapitre difficultés éthiques et méthodologie, nous sommes allés explorer l’organisation des essais en prévention dans le contexte de la PrEP à longue durée d’action.
Le coût du contrôle de l’épidémie
Cette session orale expose la problématique du coût de l’innovation thérapeutique. Nous avons choisi deux exemples qui exposent bien les questions que posent le prix des ARV à longue durée d’action, d’une part en PrEP, ici en Afrique du Sud, et d’autre part en termes d’accès au traitement dans les pays habitués au prix des génériques. Ces recherches contribuent à notre compréhension des aspects économiques des stratégies de lutte contre le VIH et soulignant le besoin crucial d’approches rentables et spécifiques au contexte pour lutter efficacement contre l’épidémie de VIH.
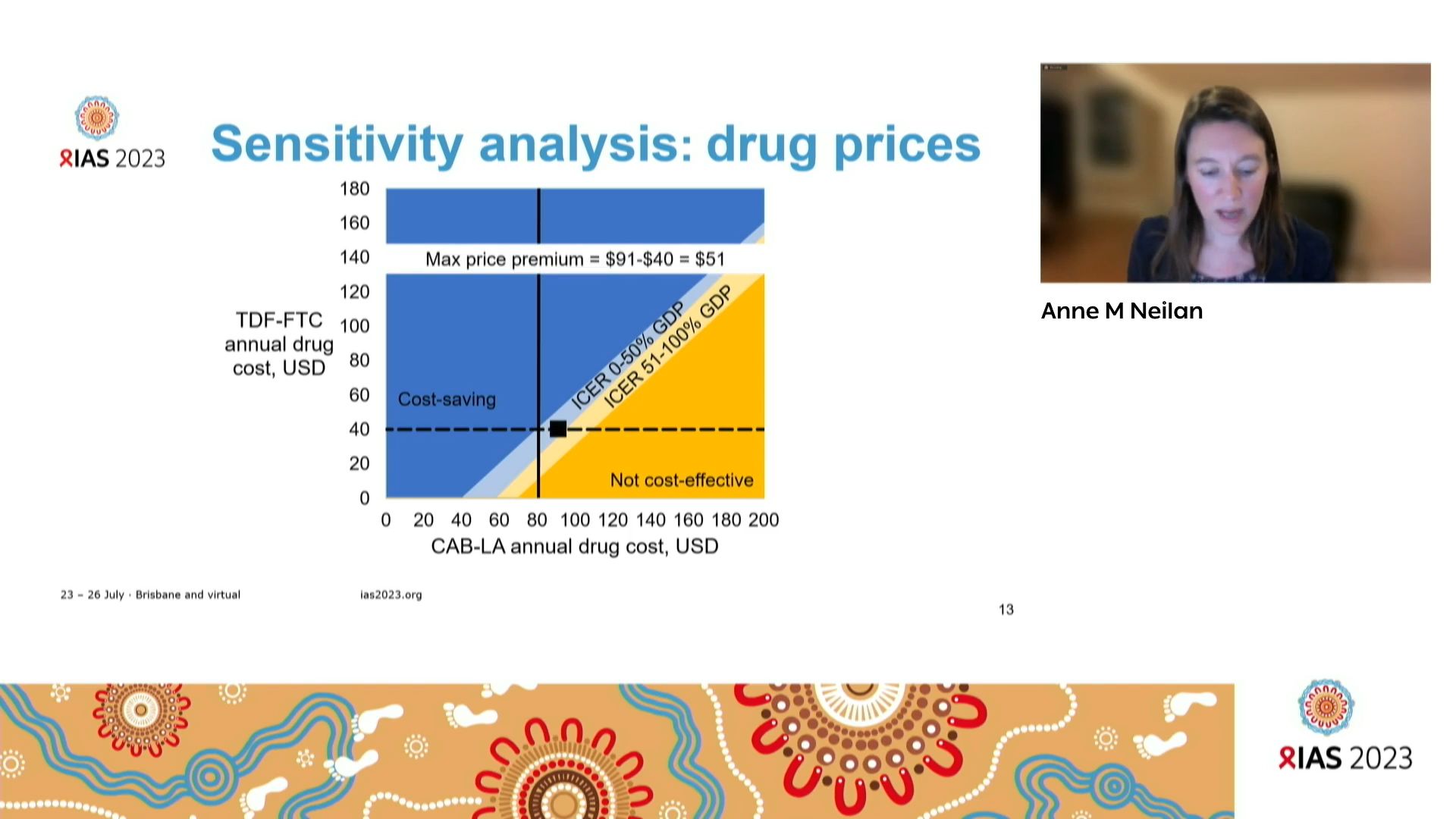
Long-acting HIV pre-exposure prophylaxis (PrEP) among adolescent girls and young women (AGYW) in South Africa: cost-effective at what cost?
Parmi les populations vulnérables qu’il est essentiel de protéger en Afrique du Sud, les adolescentes et jeunes femmes sont une cible privilégiée pour l’accès à la PrEP. Anne M NEILAN, Massachusetts General Hospital, United States, a étudié à quel prix la PrEP par injectable à longue durée d’action serait coût-efficace dans ce pays. En effet, bien que la PrEP quotidienne orale (TDF/FTC) soit accessible au faible coût des génériques, l’impérieuse nécessité d’une observance sans faille pour les femmes souligne l’intérêt qu’il y aurait à implémenter des solutions alternatives des ARV à longue durée. L’objectif de cette étude est donc de savoir quel prix du cabotegravir injectable à longue d’urée d’action (CAB-LA) en PrEP serait acceptable en termes de service rendu comparé au TDF/FTC générique oral quotidien pour les adolescentes et jeunes femmes. Cette population peut être considérée comme la plus à risque dans le contexte sudafricain avec une incidence du VH particulièrement élevée, de 3 à 7/100 personnes années. Prévenir d’une infection qu’il faut traiter à vie représente donc un enjeu de santé qui a un coût. Le groupe de chercheurs a construit ainsi un modèle d’étude à partir des données de terrain recueillies à Cape-Town, le programme FastPrEP, sur un modèle d’analyse américain de coût-efficacité de la prévention du sida (CEPAC).
Il ressort de cette étude qui évalue l’enjeu sur 10 ans, que le CAB-LA comparé au TDF/FTC serait coût efficace chez de adolescentes et jeunes femmes en Afrique du Sud pour prévenir du VIH si son prix ne dépassait pas au maximum le double du prix actuel du TDF/FTC quotidien. C’est à un prix de cet ordre que le CAB-La pourra garantir un résultat et un accès équitable à ces adolescentes en jeunes femmes à haut risque du VIH en Afrique du Sud.
Predicted HIV acquisition rates for cabotegravir versus TDF/FTC as PrEP in Brazil: effects of compulsory licensing.
La question que pose Andrew HILL, University of Liverpool, United Kingdom, à travers une enquète, c’est comment le Brésil peut se permettre d’utiliser le CAB-LA en PrEP pour mieux contrôler l’épidémie de VIH en dépit du coût élevé que cela représente et en regard du budget allouable dans ce pays. L’ONUSIDA estime le nombre de nouvelles infections annuelles au Brésil à 49 000 par an, et en estimant l’incidence à 5% dans les groupes les plus à risque, il faudrait au moins que 1,6 millions de personnes aient accès à la PrEP pour réduire drastiquement l’incidence avec une PrEP orale TDF/FTC partant de ce qu’il faut 33 personnes sous PrEP pour éviter une contamination selon les grands essais de PrEP (iPrEx, PROUD, IPERGAY). Au Brésil, ce sont 51 000 personnes qui sont sous PrEP (fin 2022) avec un budget prévention de 6 millions de dollars par an. Les données de l’essai HPTN083 (CAB-LA vs TDF/FTC) donne quant à lui une valeur de 22 personnes pour éviter une contamination. Mais voilà. Le prix du CAB-LA est aujourd’hui à 22 200$/an aux USA, 9275$/an au Royaume uni alors que son coût raisonnable de production générique est estimé par la Clinton Health Access Initiative (CHAI) à 30$/an. En juillet 2022, ViiV-Healthcare (le détenteur du brevet du CAB-LA) et l’organisation Medicines Patent Pool (MPP) ont signé un accord de cession de licence volontaire pour permettre l’utilisation générique du CAB-LA en PrEP par les pays à faible et moyenne ressource. L’accès mis en place concerne 90 pays, essentiellement l’Afrique, l’Indonésie, l’Asie du Sud-Est et l’Inde et en Amérique du Sud, un seul pays, la Bolivie. Cela signifie que sont exclus des pays comme l’Equateur, la Colombie, le Pérou, la Thaïlande, le Brésil ou la République Dominicaine alors que leur PNB est du même ordre que la Namibie, l’Afrique du Sud, le Botswana, le Gabon ou la Guinée Equatoriale qui sont dans l’accord.
A partir de ces données, les hypothèses qui se présentent au Brésil sont les suivants : 1) pas de PrEP,, 2) TDF/FTC à la demande à 12£/an, 3) TDF/FTC continu à 50$/an (prix PAHO), 4)CAB-LA à 3500$/an (66% en dessous du prix UK), 5) CAB-LA à un prix estimé de 250$, 6) CAB-LA au prix cible de CHAI de 30£/an. Avec 6 millions de $ de budget annuel pour la prévention le Brésil cible 250 000 HSH à haut risque de VIH chez qui l’incidence annuelle est la plus élevée, 5%. Il faut compter 18$ de test et counselling par personne. Si l’utilisation de TDR/FTC en PrEP permet 70% de réduction de l’incidence, le CAB-LA réalise un gain de 66% supplémentaire. Le budget d’aujourd’hui permet donc de prendre en charge 230 769 personnes/an au meilleur prix et 1707 au prix actuel du CAB-LA. A ces conditions, l’utilisation du CAB-LA en PrEP signifie l’augmentation de l’incidence du VIH. Il ne sera possible d’en tirer un bénéfice substantiel seulement si le prix est inférieur à 30$/an. Face à l’exclusion du Brésil et d’autres pays d’Amérique du Sud de l’accord ViiV-MPP malgré leurs niveaux de revenus comparables au pays qui sont dans l’accord, il reste une solution, la mise en place d’une licence obligatoire telle que prévue par l’Organisation Mondiale du Commerce.

ARV injectables pour le traitement et la prévention
Après la question du coût, nous nous sommes intéressées à la question de l’implémentation. Il ne suffit pas de rendre les produits abordables, encore faut-il pouvoir les proposer aux plus nécessiteux. Dans cette session, il est question de deux aspects essentiels de l’implémentation : d’une part, il faut se poser la question de savoir comment faire à ce que les personnes les plus difficiles à atteindre bénéficient eux-aussi des progrès de la médecine ; et d’autre part, l’amélioration de la prévention passe aussi par des solutions plus innovantes en matière d’aller vers et de simplification de la dispensation des solutions.
Implementation in hard-to-reach populations
Monica GANDHI, University of California San Francisco, United States, s’intéresse aux données du monde réel et aux aspects pratiques de l’utilisation des ARV injectables à longue durée d’action (LAI) dans le traitement du VIH. Elle décrit brièvement les études FLAIR, ATLAS et ATLAS 2M, citant leur taux d’échec virologique de 1,4 %, en grande partie dû à la résistance aux inhibiteurs de l’intégrase et/ou aux inhibiteurs non nucléosidiques de la transcriptase inverse (INNTI). Cependant ces essais ont exclu les personnes plus difficiles à soigner pour lesquelles il existe un besoin critique à les étudier. Ces populations « difficile à atteindre », constituant des groupes à l’importance critique pour atteindre la fin de l’épidémie, celles que l’on considère comme les « 10% des personnes vivant avec le VIH détenant 90% du virus » soulèvent des défis multiples et concomitants. Elle décrit ensuite l’utilisation du LAI (cabotegravir/rilpivirine) pour le traitement du VIH dans le projet WARD 86 de démonstration auprès de populations difficiles à atteindre en Californie, aux États-Unis. Les patients sont confrontés à des problèmes d’observance et souffrent de pauvreté, de maladie mentale, de logement marginal et/ou de toxicomanie. Contrairement aux études FLAIR/ATLAS, ce projet de démonstration ne requiert pas le contrôle de la charge virale à l’inclusion, mais exclut les patients présentant des mutations CAB/RPV. Les données de 133 patients montrent un taux d’échec virologique de 1,5 %, à égalité avec les études cliniques classiques. Après quelques considérations cliniques sur l’utilisation de ces thérapies et sur le prochain LAI à venir, Lenacapavir/cabotegravir, elle conclue que face aux études classiques des LAI qui limitent leur champ d’application, l’extension de l’étude de ces thérapies aux personnes « hors du champ » permettent d’étendre leur accès. Cela plaide en faveur d’études pus inclusives qui tiennent compte des besoins des populations réelles.

Long-acting injectables: opportunities and realities
Andrew MUJUGIRA, Infectious Disease Institute, Uganda, a souligné la nécessité d’approches innovantes de prestation de services différenciés pour fournir des injectables à longue durée d’action compte tenu des limites actuelles quant au lieu et par qui ces thérapies sont administrées (par les prestataires de soins de santé, dans les hôpitaux/cliniques). Il note le besoin critique de LAI parmi les personnes mobiles et vulnérables telles que les migrants. Des programmes de délivrance directe par les pharmacies de PrEP orale se sont révélés prometteurs au Kenya (CROI 2023 #978). Deux études sur la PrEP injectable délivrée par des pharmacies sont en cours en Afrique du Sud (étude AXIS) et à Seattle, Washington, États-Unis (Kelly Ross Pharmacy), ce qui pourrait fournir des informations intéressantes sur ce mode de délivrance. Le succès de la fourniture d’injectables à longue durée d’action dépendra grandement de la rapidité des approbations réglementaires, des programmes nationaux de fourniture de thérapies, du coût, des barrières d’assurance, des limites de la chaîne d’approvisionnement et de l’équité en matière de santé. Il appelle à de vastes études scientifiques de mise en œuvre pour examiner la livraison des LAI dans le cycle du produit afin d’éviter les pénuries et pour inclure des études de rentabilité.
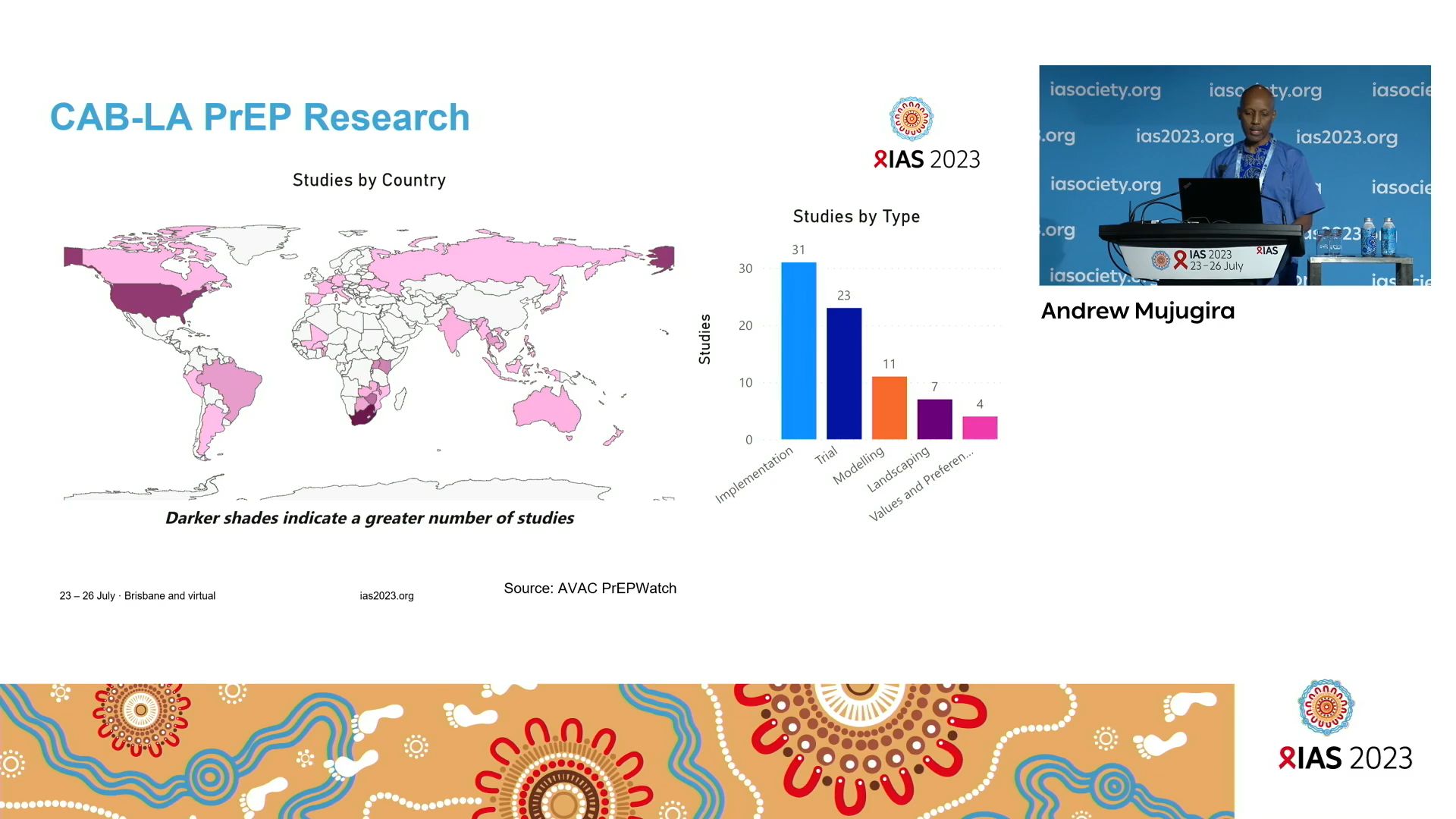
Pour conclure cette session, l’on peut dire que : alors que des taux élevés de suppression virologique ont maintenant été démontrés avec les injectables à action prolongée, la capacité à atteindre 95-95-95 d’ici 2030 dépendra de la capacité à atteindre les populations qui ont le plus besoin de ces thérapies. Les études d’efficacité en cours doivent inclure des populations « difficiles à atteindre » telles que les personnes virémiques vivant avec le VIH. Le défi est d’être capables de fournir ces thérapies à grande échelle et cela, plus tôt dans le cycle du produit.
Notre choix de présentations qui marquent l’actualité
Dans l’actualité des recherches, deux présentations ont retenu notre attention :
- La première présentation a fait partie d’une session dite co-chair choiceautrement dit, le choix des coprésidents. Dans le contexte de cette conférence très marqué par les traitements de longue durée, il n’était pas étonnant que le choix se soit porté vers le dernier résultat d’un essai d’un nouveau traitement de longue durée, ici l’association Islatravir/Doravirine. Elle a été donnée par Jürgen ROCKSTROH, le célèbre clinicien chercheur allemand de Bonn.
- La deuxième présentation est celle donnée par Asier SAEZ-CIRION dans la séance de communications tardives de recherche fondamentale (track A) et qui concernait un nouveau cas de guérison du VIH remarquable. Asier est un chercher français très impliqué dans la recherche sur la guérison du VIH. Son éclairage sur ce cas quelque peu médiatisé à l’occasion de la conférence de l’IAS méritait d’être suivi.
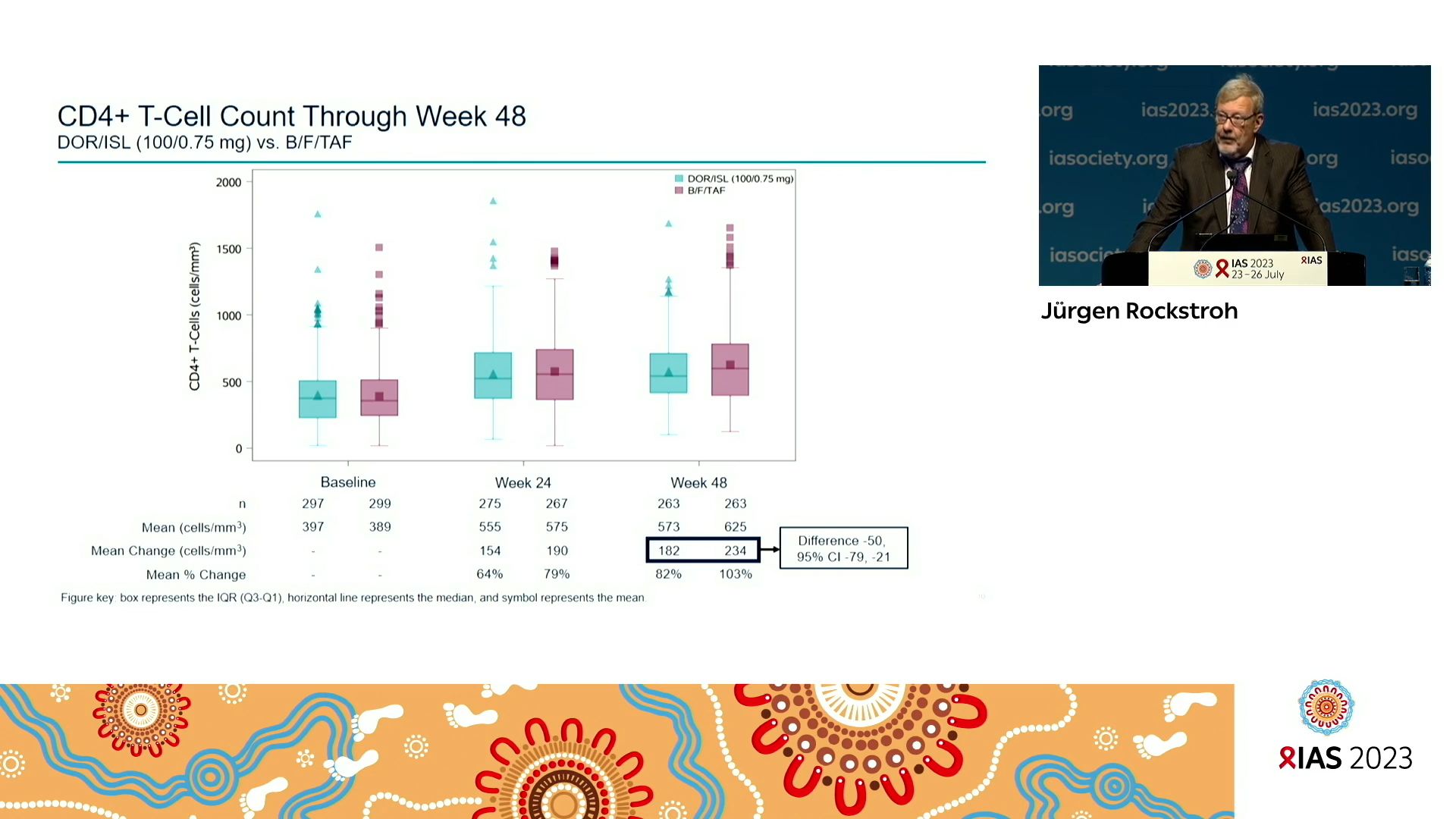
Doravirine/Islatravir (100mg/0.75mg) once daily compared to bictegravir/emtricitabine/tenofovir alafenamide (B/F/TAF) as Initial HIV-1 treatment: 48 week results from a double-blind phase 3 trial
Jürgen ROCKSTROH, University of Bonn, Germany, a présenté les résultats sur 48 semaines de MK8591A-020, un essai clinique de phase 3 en double aveugle comparant Doravirine/Islatravir 100 mg/0,75 mg (DOR/ISL) une fois par jour à bictégravir/emtricitabine/ténofovir alafénamide (B/F/ TAF) comme traitement initial du VIH-1. DOR/ISL n’était pas inférieur à B/F/TAF pour atteindre un ARN VIH-1 plasmatique inférieur à 50 copies/mL à 48 semaines. 1 participant du groupe DOR/ISL a développé une résistance à la doravirine du fait d’une non-observance du traitement. DOR/ISL a été généralement bien toléré, mais avec un niveau inférieur de lymphocytes T CD4+ et une augmentation des lymphocytes totaux à la semaine 48.
L’essai MK8591A-020 a montré un taux plus élevé de chute du nombre de lymphocytes dans le groupe DOR/ISL, mais aucune analyse statistique de cette tendance n’a été effectuée. Après la suspension des essais de l’islatravir du fait de la baisse de lymphocytes T CD4+ les essais en cours impliquant DOR/ISL ont repris mais avec une dose plus faible d’islatravir à 0,25 mg.
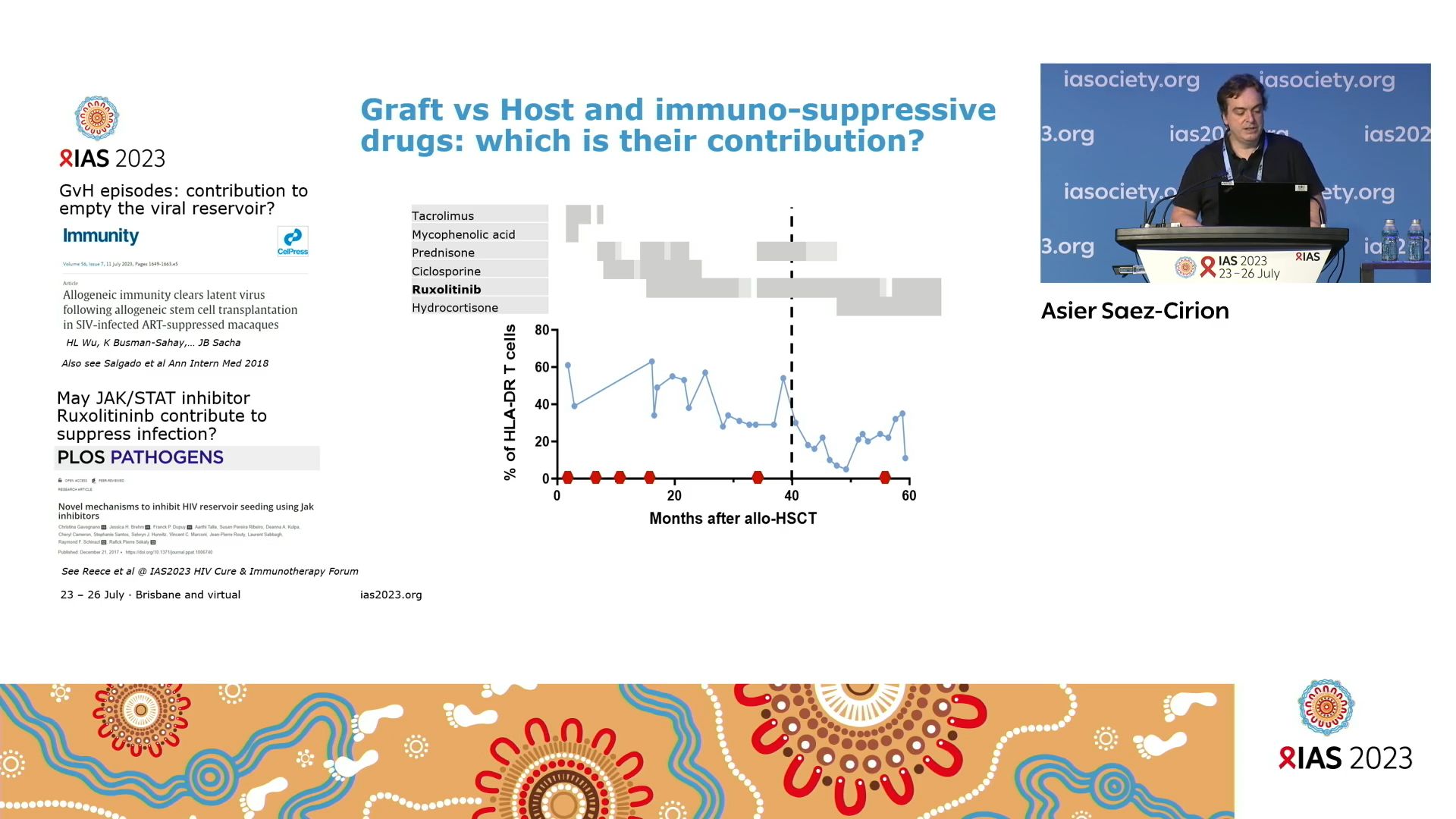
Absence of viral rebound for 18 months without antiretrovirals after allogeneic hematopoietic stem cell transplantation with wild-type CCR5 donor cells to treat a biphenotypic sarcoma
Asier SAEZ-CIRION, Institut Pasteur, a présenté une étude dans laquelle une personne vivant avec le VIH a reçu une greffe de cellules souches d’un donneur en raison d’un sarcome. Contrairement à d’autres cas de guérison du VIH, les cellules du donneur étaient de type sauvage CCR5, c’est-à-dire qu’elles ne présentaient pas de résistance naturelle au VIH. Pour autant aucun rebond viral n’a été observé pendant 20 mois après l’arrêt du traitement antirétroviral. D’autres marqueurs du réservoir du VIH sont également devenus indétectables.
Jusque-là, 5 personnes vivant avec le VIH avaient eu recours à une greffe de moelle osseuse pour des raisons thérapeutiques graves du même ordre et avaient été considérées comme guéries du VIH. Mais dans tous les cas les donneurs étaient porteurs de la mutation CCR5∆32 qui confère aux cellules une résistance naturelle à l’entrée du VIH. On considérait donc que la mutation était un facteur essentiel pour obtenir la guérison par le biais de la greffe. Dans le cas présent, les raisons de l’absence de rebond viral sont à chercher ailleurs. Parmi les questions qu’il faut se poser, il y a : 1) la greffe est-elle suffisante pour éliminer toutes les cellules du réservoir ? 2) quelle a été la contribution des cellules NK au contrôle de l’infection ? 3) quel est le rôle joué par les médicaments immunosuppresseurs utilisés dans le protocole thérapeutique qui accompagne la greffe, en particulier, le ruxolitinib a-t-il permis la suppression des évènements de réactivation virale ?
La démonstration de l’absence de rebond viral après une greffe de cellules souches avec des cellules de type sauvage CCR5 pourrait-elle en faire une option de traitement du VIH plus viable ?
Estimer l’incidence du VIH à l’ère de la PrEP à longue durée d’action
Ce qui se cache derrière ce titre, est la poursuite d’une longue discussion méthodologique des essais de prévention. Pour celles et ceux qui ne sont pas familiers de ce débat récurrent, et pour mieux appréhender les enjeux de cette session, voici un rappel des étapes précédentes. Les essais en prévention de la transmission du VIH ont commencé il y a longtemps par des essais vaccinaux. Quand il s’est agi de passer à la phase III, d’efficacité, ces essais ont été conduits selon le mode vaccin vs placebo. Au début des années 90, une étude observationnelle sur la transmission par accident d’exposition chez les soignants avait conclu à une efficacité substantielle du TPE ou prophylaxie post-exposition. Mais aucun essai clinique n’est venu étayer ce résultat parce qu’il avait été considéré comme in-éthique de le faire. C’était le début de la prévention biomédicale encore que, à la même époque, les premiers essais de prévention de la transmission mère-enfant ont été conduits. Et puis au début des années 2000 est arrivé l’idée de la PrEP. Tout naturellement les essais de cette décennie ont été menés sur le mode traitement vs placebo. En fait, pas tout à fait. Après les tout premiers essais un large débat avait été lancé (IAS 2005) sur l’éthique dans les essais de prévention biomédicale dans lequel on avait conclu que « le meilleur standard de prévention » devait être proposé aux participants, en l’occurrence à l’époque le préservatif. Et puis iPrEx a donné le premier résultat probant sur la PrEP en 2012. Juste au moment où se lançaient les essais IPERGAY et PROUD. Le premier sur le mode intervention vs placebo a été beaucoup critiqué mais s’est déroulé comme prévu, le deuxième a choisi pour cela une méthodologie subtile de comparaison entre une cohorte observationnelle et une cohorte sous PrEP. A partir des résultats probants de ces deux essais, il était clair que « le meilleur standard de prévention » devenait la PrEP par TDF/FTC. C’est pourquoi les essais suivants, notamment d’homologation du cabotegravir en PrEP se sont faits par comparaison avec la PrEP validée, TDF/FTC. Qu’en est-il des essais vaccinaux ? Le principe éthique veut qu’ils soient conduits par comparaison à la PrEP. Mais voilà. Compte tenu de l’efficacité de cette dernière, elle risque de ne pas permettre d’observer les effets d’un vaccin qui serait notamment moins efficace et pose la question de la poursuite ou non de la PrEP chez les participants au-delà de l’essai. D’où la nécessité pour les chercheurs de trouver des mécanismes de substitution pour poursuivre les recherches, autrement dit, être capable d’estimer l’incidence du VIH dans un groupe soumis à un essai interventionnel de prévention autrement qu’en comptant les contaminations. Voilà le décor est planté, place aux orateurs.
Novel scientific approaches for establishing efficacy of new biologics in the era of long-acting PrEP
Deborah DONNELL, Fred Hutchinson Cancer Research Center, United States, a commencé la séance en donnant un aperçu de l’utilisation d’un « placebo contrefactuel » – contrefactuel est un néologisme, traduction de l’anglais counterfactual, on pourrait le traduire aussi par « contrefait » ou « de substitution » – pour estimer l’incidence de fond du VIH et calculer l’efficacité des nouveaux agents lorsque l’incidence du VIH dans les groupes de contrôle et expérimental est similaire. Les estimations de l’incidence pourraient provenir d’autres essais, de cohortes d’enregistrement, de tests d’infection récente, de prédicteurs fiables du risque de VIH, ou de l’observance ou de biomarqueurs immunitaires. Ces approches reposent toutes sur des faisceaux d’hypothèses. Au bout du compte, il est important de s’assurer que la preuve apportée par un essai d’efficacité d’un nouvel agent est fiable même lorsqu’on dispose de multiples options de prévention dont l’efficacité est prouvée. En conclusion, l’efficacité estimée à partir de l’approche du placebo contrefactuel permet de progresser dans la recherche de nouveaux agents préventifs. Il demeure indispensable d’aborder ces aspects avec les autorités de régulation, les investigateurs, les biostatisticiens et les parties prenantes communautaires. A porter à la discussion, le document de la FDA : “Considerations for the Design and Conduct of Externally Controlled Trials for Drugs and Biological Products” Draft guidance 2023.
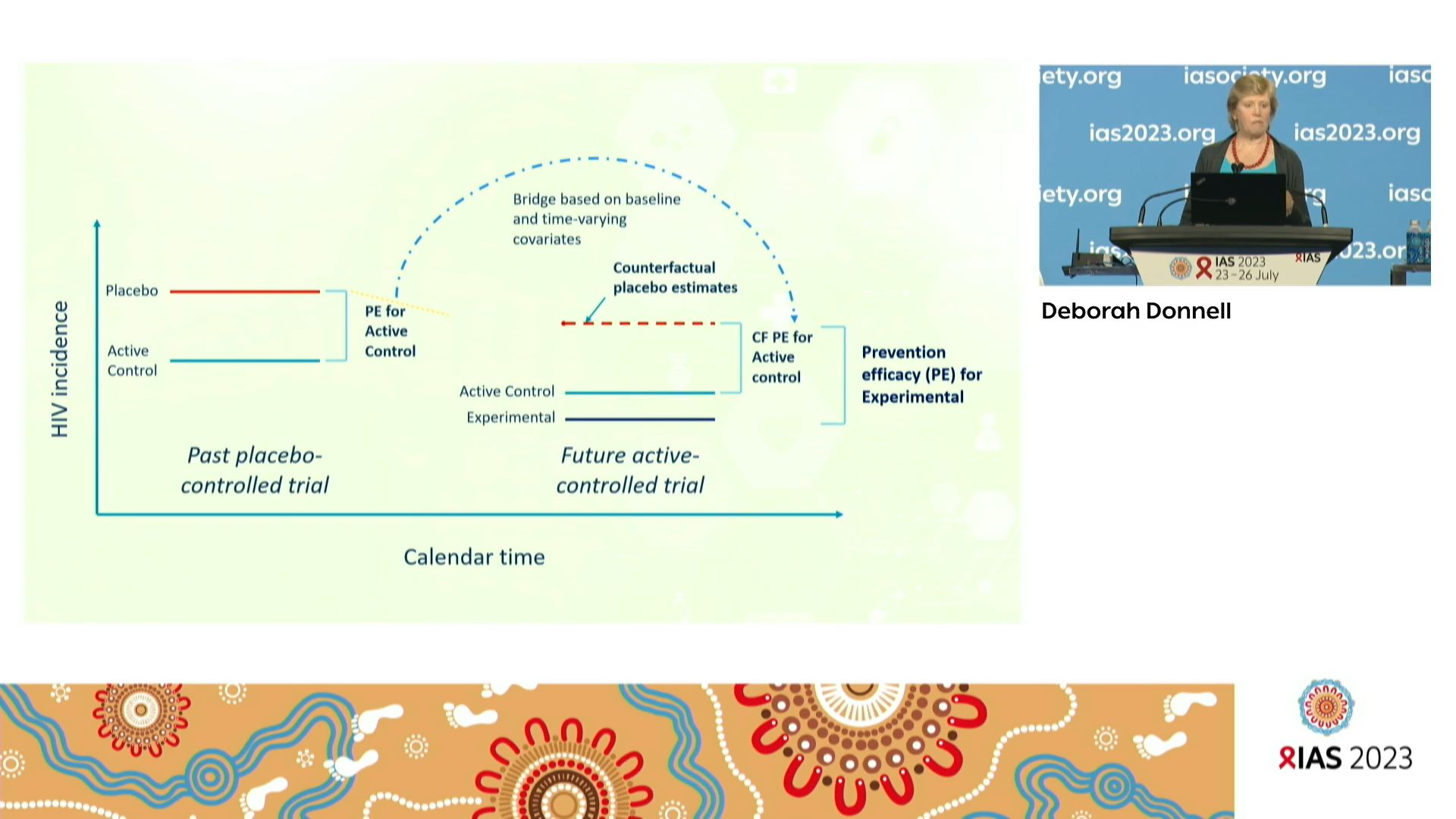
Experience with using recency assays to estimate HIV incidence in an HIV prevention trial
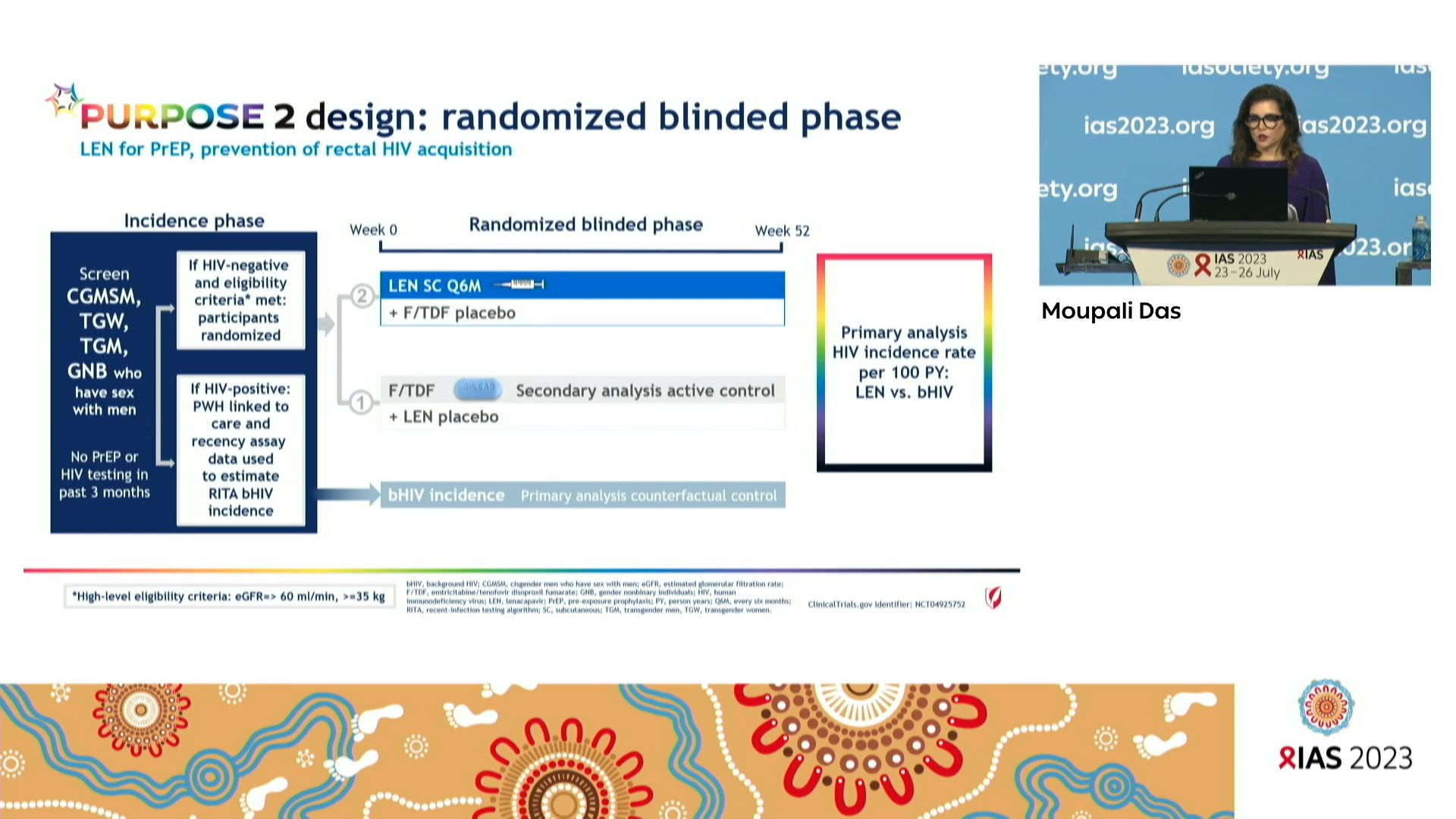
Deborah Donnell Moupali DAS, Gilead Sciences, United States, a fait une présentation sur l’utilisation des algorithmes de dépistage des infections récentes pour estimer l’incidence de fond du VIH pour les études Purpose du Lenacapavir pour la PrEP et la prévention du VIH vaginal et rectal.
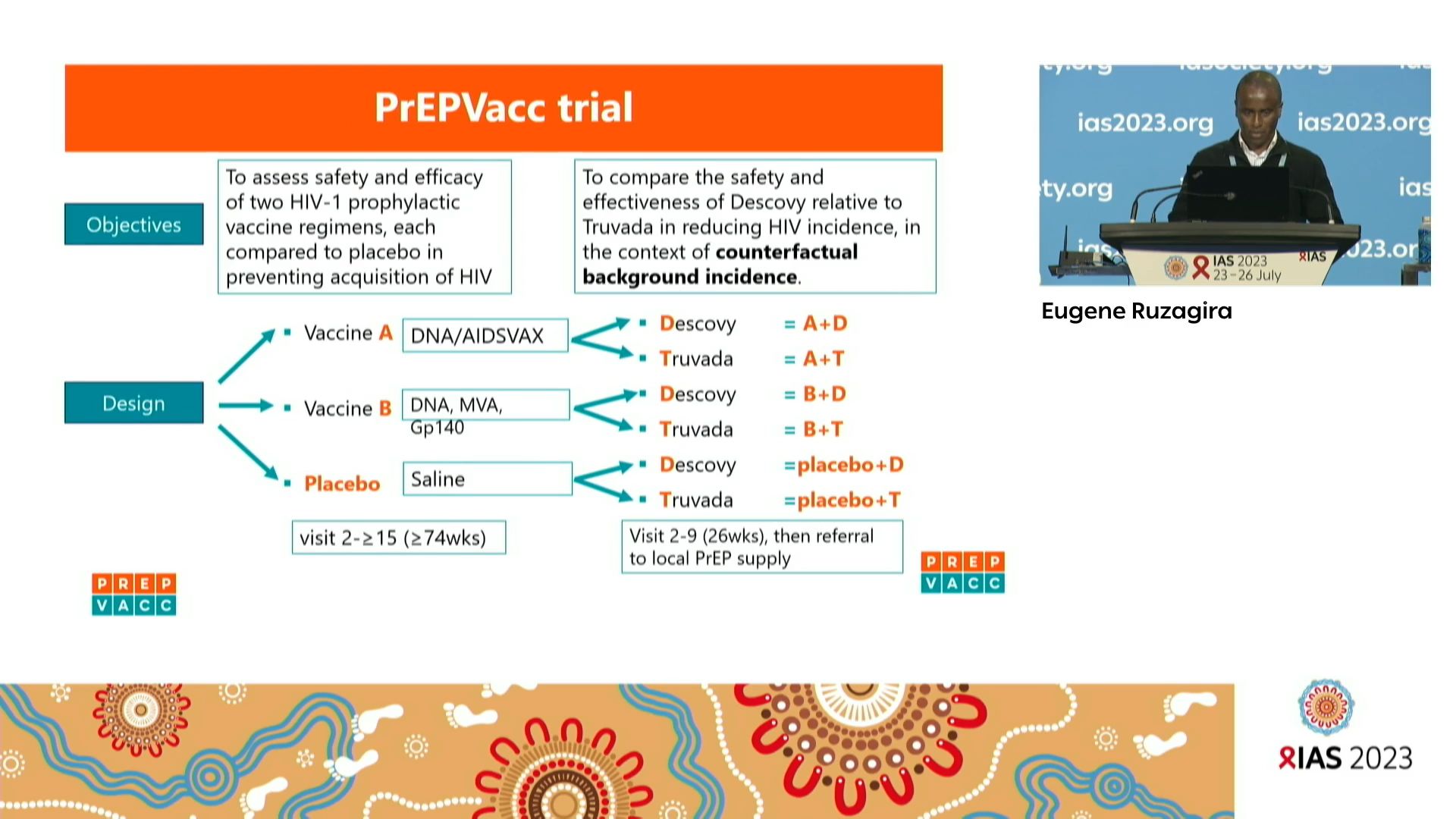
Experience with using a registrational cohort to estimate HIV incidence: Lessons from PREPVAcc
Eugene RUZAGIRA, MRC/UVRI and LSHTM Uganda Research Unit, Uganda, a ensuite décrit l’utilisation d’une cohorte d’enregistrement pour estimer l’incidence de fond du VIH pour l’essai PrEPVacc. L’incidence estimée du VIH a montré une baisse au fil du temps et a été affectée par un groupe de séroconversions et de restrictions liées au COVID-19, soulignant les défis liés à l’utilisation de ces méthodes d’estimation.
La table ronde a mis en évidence les complexités et les aspects pratiques de la conduite d’essais à l’ère des traitements hautement efficaces, des agents de prévention et à l’ère de la prévention combinée. Parmi les questions qui sont loin d’être résolues, celle qui émerge est de savoir ce qu’est vraiment l’incidence de fond du VIH. Définissable en premier lieu comme l’incidence qui existe en l’absence d’intervention, on se rend très vite compte qu’elle est éminemment dépendante du contexte environnant. Dans une épidémie forte, l’exposition est forte, et inversement. Dans une société où la PrEP existe, l’incidence va dépendre de l’effectivité collective de la prévention.
Il est important que des conceptions d’essais innovantes soient développées afin que l’efficacité d’une nouvelle PrEP et d’autres agents de prévention puisse être évaluée de manière robuste, efficace et éthique. Les différentes approches décrites dans cette session sont prometteuses, mais elles reposent toutes sur des hypothèses qui pourraient affecter la robustesse des résultats des essais et plusieurs défis pratiques devront être surmontés. Cela inclut la possibilité d’obtenir l’approbation réglementaire pour le déploiement de nouveaux agents. Il est probable que plusieurs approches seront nécessaires pour l’application dans les essais qui pourraient varier selon les contextes et les populations.
Tous les articles IAS 2023 à retrouver ici :
- IAS 2023, tous les sujets en plénière -1-
- IAS 2023, tous les sujets en plénière -2-
- IAS 2023 : d’autres sessions, morceaux choisis
L’article introductif :
